近日,我室刘惠玉教授团队和中国医学科学院肿瘤医院分子肿瘤学国家重点实验室马洁、袁伟研究员团队合作,开发了一种可降解碳-二氧化硅纳米复合材料(CSN),可在生理介质中实现无酶降解并具有光热/光动力和激活树突状细胞的免疫佐剂性质,实现高效抗肿瘤治疗。相关成果发表于ACS Nano(DOI: 10.1021/acsnano.9b06168),并被遴选为当期的Supplementary Journal Cover。刘惠玉教授和袁伟研究员为本文的通讯作者,有机无机复合材料国家重点实验室为第一署名单位。
纳米光控治疗如光热疗法(PTT)和光动力疗法(PDT)具有适用范围广、低侵入性、过程简便等优点,在肿瘤治疗领域展现出巨大的应用前景。近年来,多种纳米材料被报道具有PTT和PDT双光疗特性。其中,碳基纳米材料因其易于制备、高光热转换效率而备受关注。然而,常用碳基纳米材料不易降解的问题严重阻碍了其临床应用,开发具有可降解性能的高效光疗碳基材料是将光疗抗癌技术推向临床的难点之一。为此,团队采用树枝状生物降解介孔二氧化硅为模板负载不连续相碳结构,构建了可降解介孔碳硅纳米颗粒(CSN),该生物材料优势如下:1)在近红外光照射下,CSN可在生理介质中实现无酶降解;2)具有光热/光动力性质和光声(PA)成像功能,用于成像引导的双模肿瘤光疗;3)CSN免疫佐剂特性可以激活树突状细胞(DCs),光疗可进一步增强DCs熟化及抗肿瘤免疫应答。
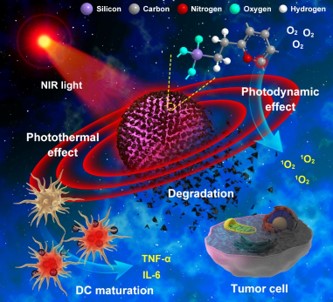
图1 具有免疫佐剂性质的可降解CSN用于癌症治疗的示意图
团队不仅在乳腺癌皮下瘤模型上验证了CSN的治疗效果与免疫佐剂性质,还在人源性组织异种移植(PDX)模型上进一步探索了CSN的治疗效率。与传统细胞系异种移植模型不同,PDX模型来源于患者手术或穿刺得到的新鲜实体瘤,该模型不仅保留了人类原发癌组织的肿瘤内异质性和组织学特征,还再生了包含脉管系统,细胞外基质和肿瘤基质成纤维细胞的肿瘤微环境,利于更好的表现亲代肿瘤性状,并维持了肿瘤的异质性,因此无论从组织病理还是分子病理,都十分接近病人,对癌症治疗的临床前评价具有积极意义。
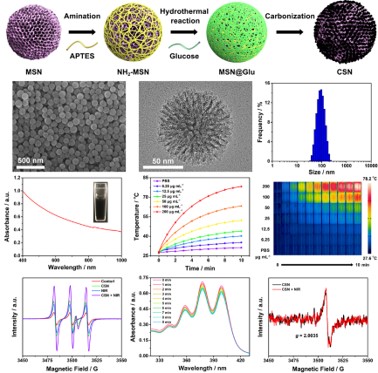
图2 CSN的制备,形貌和光疗性能表征
要点: CSN是一种分散性好、粒径均一,具有介孔结构以及对NIR光具有较高吸收的碳硅材料。其光热转化效率约为34.5%,并可NIR光的照射下可以产生单线态氧。
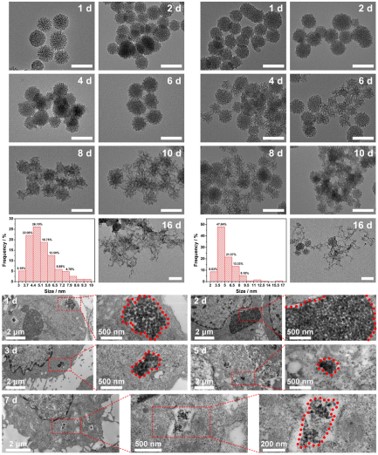
图3 CSN在体外模拟生理条件以及在细胞内环境的降解行为
要点:CSN在模拟体液和模拟溶酶体液中,经NIR光照射可以在16天内无酶降解为~5 nm的小颗粒,且在细胞内也可以降解。
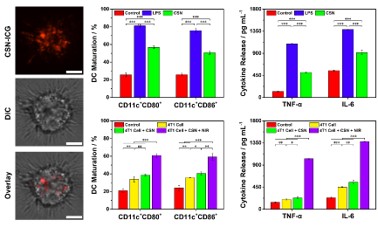
图4 CSN诱导树突状细胞活化并分泌细胞因子
要点:CSN具有免疫佐剂性质,可以非特异性激活DCs,分泌细胞因子。光疗后可进一步增强激活DCs分泌细胞因子,引发后续的抗肿瘤免疫反应。
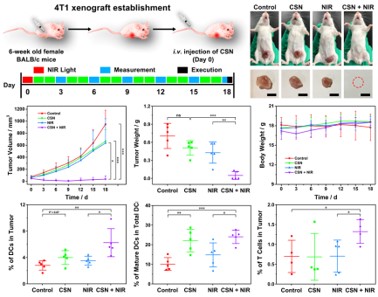
图5 验证CSN在4T1模型中的抗肿瘤效果及体内免疫佐剂性质
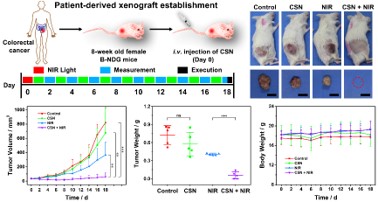
图6 验证CSN在PDX模型中的抗肿瘤效果
要点:CSN在4T1皮下瘤模型中实现了93.2%的肿瘤抑制率。此外,CSN可以在体内激活肿瘤浸润的DCs,光疗后可进一步促进DCs在肿瘤中的积累和活化,以及更多的T细胞浸润,增强抗肿瘤免疫作用。
在免疫缺陷鼠上建立了PDX模型,并探索了CSN的治疗效果,实现了92.5%的肿瘤抑制率,对癌症治疗的临床前评价具有积极意义。
论文链接:https://pubs.acs.org/doi/10.1021/acsnano.9b06168
刘惠玉课题组网页:http://www.liuhuiyugroup.com
